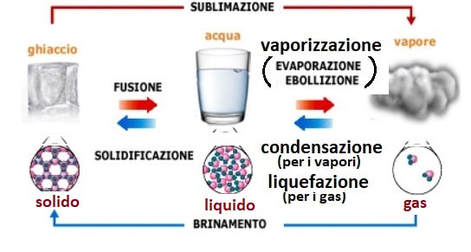
PASSAGGI DI STATO DELLA MATERIA
QUANDO AVVENGONO I PASSAGGI DI STATO DELLA MATERIA
Ogni sostanza può esistere in ognuno di questi stati e quindi può passare da uno stato ad un altro; questi passaggi si chiamano appunto passaggi di stato. Essi sono:
LA FUSIONE ( passaggio da solido a liquido)
Quando si riscalda un solido la sua temperatura aumenta. Questo significa che le molecole compiono oscillazioni sempre più ampie e veloci intorno alle loro posizioni di equilibrio nel reticolo cristallino. Nel momento in cui si arriva alla temperatura di fusione, l’agitazione termica delle particelle è tale che il reticolo comincia a rompersi. Per tutta la durata della fusione, il calore che viene somministrato dall’esterno non viene utilizzato per far aumentare la temperatura, ma per rompere il reticolo cristallino. Solo quando tutto il solido si è trasformato in liquido è possibile fare aumentare la temperatura del sistema. Generalmente la fusione è caratterizzata da un aumento di volume.
LA VAPORIZZAZIONE (passaggio da liquido ad aeriforme)
Può avvenire in due modi: evaporazione ed ebollizione.
Di questi due fenomeni, soltanto l’ebollizione presenta tutte le caratteristiche di un passaggio di stato, perché avviene ad una temperatura fissa per ogni sostanza, e la temperatura del sistema resta costante per tutta la durata del passaggio di stato.Man mano che si fornisce calore a un liquido, l’agitazione termica delle sue particelle aumenta.
Quando si raggiunge la temperatura di ebollizione, l’agitazione termica è tanto forte che il suo effetto prevale sulle forze di attrazione fra le molecole del liquido; le molecole, quindi, si separano l’una dall’ altra, e passano allo stato di vapore.L’evaporazione è un processo più lento, avviene a qualsiasi temperatura e interessa solo la superficie del liquido: sono cioè le molecole della superficie che un po’ alla volta si staccano dalle loro vicine e si mescolano all’aria.
Più la temperatura dell’ambiente è elevata, più velocemente avviene l’evaporazione.Inoltre, siccome il fenomeno interessa solo la superficie del liquido, più ampia è questa superficie più rapidamente avviene l’evaporazione.
LA LIQUEFAZIONE (passaggio da aeriforme a liquido)
Per farla avvenire senza variare la pressione, bisogna raffreddare il gas fino alla temperatura di liquefazione. A questo punto il gas comincia a condensare formando goccioline di liquido, cioè le molecole del gas cominciano a formare dei legami fra loro, a unirsi l’una all’altra: si formano così le goccioline di liquido. Se si continua a raffreddare la temperatura non cambia, ma una quantità sempre maggiore di gas si trasforma in liquido. Soltanto quando tutto il gas è divenuto liquido è possibile fare abbassare la temperatura del liquido, se si continua a sottrarre calore. Durante la liquefazione la temperatura rimane costante, perché il calore che viene sotratto dall’esterno con il raffreddamento è compensato dal calore che si sviluppa nel processo di formazione del liquido, cioè nella formazione di legami fra una molecola e l’altra.
LA SOLIDIFICAZIONE (passaggio da liquido a solido)
Quando un liquido viene raffreddato, la sua temperatura si abbassa. Quando raggiunge la temperatura di solidificazione il liquido comincia a trasformarsi in un solido e la temperatura non si abbassa più. Il calore sottratto con il raffreddamento viene compensato dal calore che si sviluppa nel processo di formazione del reticolo cristallino del solido. Infatti durante la solidificazione le molecole del liquido si dispongono man mano secondo la struttura ordinata propria dei solidi, e questo è un processo che sviluppa calore.
LA SUBLIMAZIONE ( passaggio diretto da solido ad aeriforme)
La sublimazione, passaggio diretto da solido a vapore, avviene soprattutto per alcune sostanze. E’esperienza comune vedere che il ghiaccio “fuma”, cioè ha intorno del vapore; quel vapore è prodotto appunto dalla sublimazione del ghiaccio. Ad esempio se lasciamo all’aria un quadretto di canfora o una pallina di naftalina, vediamo che dopo un po’ di giorni le loro dimensioni si sono ridotte; il quadretto e la pallina sono diventati più piccoli, e col passare del tempo lo diventano sempre di più, fino a scomparire; questo perché anche la naftalina e la canfora sublimano, passando lentamente allo stato gassoso. La sublimazione è tanto più intensa quanto minore e la pressione. Ci sono sostanze che non sublimano a pressione ordinaria, ma sublimano se la pressione viene diminuita. E per le sostanze che già sublimano a pressione ordinaria, l’entità della sublimazione diviene maggiore se si riduce la pressione.
BRINAMENTO (passaggio diretto da aeriforme a solido)
Il brinamento è il passaggio dallo stato aeriforme allo stato solido di una sostanza, senza passare per lo stato liquido. L'origine del termine italiano si ricollega alla brina che si forma sull'erba quando, a causa delle basse temperature, il vapore acqueo nell'aria si trasforma in aghetti di ghiaccio che si depositano sull'erba.
---------------------------------
I passaggi di stato sono fenomeni fisici, perché non danno luogo a cambiamenti nella composizione delle sostanze interessate. Ad esempio, il ghiaccio, l’acqua allo stato liquido e il vapore acqueo sono tutti costituiti da molecole di acqua, H2O; è diverso solo i modo con cui queste molecole sono unite fra di loro, o nel caso del vapore non sono unite affatto.
I passaggi di stato avvengono a temperature caratteristiche per ogni sostanza pura.
Per ogni sostanza avremo quindi una temperatura di fusione e una temperatura di ebollizione.
La temperatura a cui avviene un passaggio di stato dipende anche dalla pressione.
L’acqua pura bolle a 100 °C se la pressione è di una atmosfera.
Se la pressione è minore, come succede in alta montagna, l’acqua bolle a una temperatura inferiore.
Se invece la pressione è maggiore di una atmosfera, l’acqua bolle a una temperatura superiore ai 100°C.
E’ quello che avviene nella pentola a pressione: la cottura dei cibi è più rapida perché avviene ad una temperatura maggiore.
Abbassando fortemente la pressione è possibile far bollire l’acqua anche a temperatura ambiente.
Durante un passaggio di stato, la temperatura rimane costante fino a quando il passaggio stesso non si è completato. (calore latente)
CENNI SULLA STRUTTURA DELLA MATERIA
(la materia è fatta essenzialmente da energia Einstein E=mc2)
Tutta la materia che compone l’universo sostanzialmente si presenta ai nostri sensi sotto tre possibili aspetti. Sono questi gli STATI DI AGGREGAZIONE DELLA MATERIA e sono :
STATO SOLIDO: dove la materia ha forma e volume proprio.
STATO LIQUIDO: dove la materia ha volume proprio ma forma del contenitore che la contiene.
STATO AERIFORME: dove la materia non ha forma ne volume proprio.
Tutta la materia che compone l’universo può essere formata da singoli elementi (sostanze o atomi) oppure dall’unione di più elementi (composti o molecole). L’unione di diversi atomi e diverse molecole vanno a costituire gli infiniti materiali che ci circondano. Gli elementi stabili che in natura sono solo 92 vengono classificati nella TAVOLA PERIODICA DEGLI ELEMENTI (tavola di Mendelejeff). Oltre al 92° elemento che è l’Uranio abbiamo una serie di elementi instabili detti anche radioattivi.
LA MOLECOLA
La molecola è la parte più piccola in cui possiamo suddividere la materia che però mantiene ancora tutte le caratteristiche chimico-fisiche della sostanza iniziale (aspetto,colore, sapore, odore, temperature di fusione e di ebollizione, capacità di reagire con altri elementi ecc..) (ex. Sono molecole l’acqua H2O, il sale NaCl, lo zucchero C6H12O6, l’anidride carbonica CO2 ecc..)
L’ATOMO
L’atomo (che in greco vuol dire indivisibile) è la più piccola quantità di materia che non può essere ulteriormente scomposta con mezzi chimici.
TEORIA ATOMICA
Questa teoria tenta di spiegare come può essere composto un atomo.
Si pensa che l’atomo sia costituito da un nucleo centrale formato da PROTONI (particelle di carica positiva) e NEUTRONI (particelle senza carica). Attorno al nucleo girano su orbite ellittiche alla velocità della luce (300.000 Km/s) gli ELETTRONI (particelle di carica negativa.) Il numero di elettroni e di protoni è identico quindi l’atomo è elettricamente neutro. Il numero di neutroni all’interno del nucleo può variare dando origine ai diversi ISOTOPI che sono atomi chimicamente uguali ma con peso molecolare diverso. Per avere un’idea più concreta della struttura di un atomo, si potrebbe paragonare il nucleo ad una capocchia di uno spillo e immaginare che gli elettroni girino su di un orbita di 11 metri di raggio. E’ facile a questo punto costatare che il volume occupato dall’atomo è immenso rispetto al volume delle particelle che lo compongono. Per questo motivo si può sostenere che la materia è fatta essenzialmente da energia. Se fosse possibile far collasare gli elettroni sul nucleo (ciò potrebbe succedere alla temperatura dello zero assoluto, -273°C) l’enorme volume occupato prima dalle orbite degli elettroni, sparirebbe e per ipotesi, il nostro pianeta potrebbe divenire grande come una pallina da tennis ma mantenendo ancora tutta la sua massa iniziale. In qualche regione dello spazio siderale questo avviene spontaneamente e gli astronomi individuano queste regioni come BUCHI NERI.
(la materia è fatta essenzialmente da energia Einstein E=mc2)
Tutta la materia che compone l’universo sostanzialmente si presenta ai nostri sensi sotto tre possibili aspetti. Sono questi gli STATI DI AGGREGAZIONE DELLA MATERIA e sono :
STATO SOLIDO: dove la materia ha forma e volume proprio.
STATO LIQUIDO: dove la materia ha volume proprio ma forma del contenitore che la contiene.
STATO AERIFORME: dove la materia non ha forma ne volume proprio.
Tutta la materia che compone l’universo può essere formata da singoli elementi (sostanze o atomi) oppure dall’unione di più elementi (composti o molecole). L’unione di diversi atomi e diverse molecole vanno a costituire gli infiniti materiali che ci circondano. Gli elementi stabili che in natura sono solo 92 vengono classificati nella TAVOLA PERIODICA DEGLI ELEMENTI (tavola di Mendelejeff). Oltre al 92° elemento che è l’Uranio abbiamo una serie di elementi instabili detti anche radioattivi.
LA MOLECOLA
La molecola è la parte più piccola in cui possiamo suddividere la materia che però mantiene ancora tutte le caratteristiche chimico-fisiche della sostanza iniziale (aspetto,colore, sapore, odore, temperature di fusione e di ebollizione, capacità di reagire con altri elementi ecc..) (ex. Sono molecole l’acqua H2O, il sale NaCl, lo zucchero C6H12O6, l’anidride carbonica CO2 ecc..)
L’ATOMO
L’atomo (che in greco vuol dire indivisibile) è la più piccola quantità di materia che non può essere ulteriormente scomposta con mezzi chimici.
TEORIA ATOMICA
Questa teoria tenta di spiegare come può essere composto un atomo.
Si pensa che l’atomo sia costituito da un nucleo centrale formato da PROTONI (particelle di carica positiva) e NEUTRONI (particelle senza carica). Attorno al nucleo girano su orbite ellittiche alla velocità della luce (300.000 Km/s) gli ELETTRONI (particelle di carica negativa.) Il numero di elettroni e di protoni è identico quindi l’atomo è elettricamente neutro. Il numero di neutroni all’interno del nucleo può variare dando origine ai diversi ISOTOPI che sono atomi chimicamente uguali ma con peso molecolare diverso. Per avere un’idea più concreta della struttura di un atomo, si potrebbe paragonare il nucleo ad una capocchia di uno spillo e immaginare che gli elettroni girino su di un orbita di 11 metri di raggio. E’ facile a questo punto costatare che il volume occupato dall’atomo è immenso rispetto al volume delle particelle che lo compongono. Per questo motivo si può sostenere che la materia è fatta essenzialmente da energia. Se fosse possibile far collasare gli elettroni sul nucleo (ciò potrebbe succedere alla temperatura dello zero assoluto, -273°C) l’enorme volume occupato prima dalle orbite degli elettroni, sparirebbe e per ipotesi, il nostro pianeta potrebbe divenire grande come una pallina da tennis ma mantenendo ancora tutta la sua massa iniziale. In qualche regione dello spazio siderale questo avviene spontaneamente e gli astronomi individuano queste regioni come BUCHI NERI.





